Die Immunabwehr gegen Mikroorganismen wird mit Hilfe von zwei Verteidigungslinien geführt – die erste Verteidigungslinie, die sog. angeborene Immunität (innate immunity) reagiert schnell aber unspezifisch und wird durch bestimmte Zytokine (z.B. Typ I Interferone) und natürliche Killerzellen (NK-Zellen) vermittelt – ich hatte diese Mechanismen im letzten Beitrag ausführlicher dargestellt.
Die zweite Verteidigungslinie braucht etwas Zeit, um nach einer Infektion in Gang zu kommen, ist aber dafür wesentlich spezifischer und führt auch zu Ausbildung eines immunologischen Gedächtnisses – also einer Immunität gegen einen Erreger nach einer erneuten Infektion. Dieser Teil des Immunsystems wird als adaptive Immunitiät (adptive immunity) bezeichnet und wird u.a. durch T- und B-Lymphozyten vermittelt. (Hier sei noch kurz erwähnt, dass die T-Lymphozyten in sog. CD4 positive und CD8 positive T-Lymphozyten unterschieden werden).
Wie die adaptive Immunität gegen Viren funktioniert, möchte ich in diesem Beitrag näher erläutern. Es muss aber betont werden, dass beide Teile der Immunabwehr – angeborene und adaptive Immunität – eng zusammenarbeiten, um Viren aus unserem Körper zu eliminieren. Die hier vorgenommene Trennung hat eher didaktische Gründe.
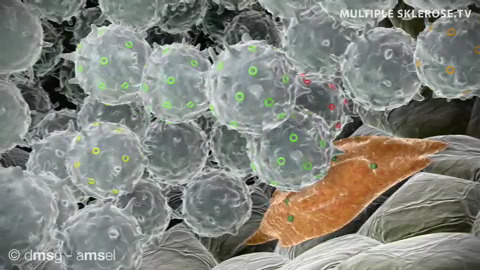
Im adaptiven Immunsystem sind die sog. zytotoxischen T-Lymphozyten (CTL = cytotoxic T-Lymphocytes) für die effiziente Abtötung von Zellen, die mit Viren infiziert sind, zuständig. Diese zytotoxischen T-Lymphozyten müssen sich aber erst entwickeln – man nennt das in der Immunologie auch Differenzierung. So differenzieren sich naive CD8 positive T-Lymphozyten (denen die Fähigkeit zum Abtöten noch fehlt) auf bestimmte Stimuli im Rahmen einer Virusinfektion zu CTLs. Die so in großer Zahl entstandenen virusspezifischen CTLs erkennen virusinfizierte Zellen dadurch, dass kleinste Bestandteile der Viren auf die Oberfläche der infizierten Zelle gelangen und die infizierten Zellen dadurch für die CTLs markieren. Innerhalb des Zytoplasmas differenzierter CTLs befinden sich zahlreiche Granula, die Proteine enthalten wie Perforin und Granzym, mit deren Hilfe eine Zielzelle abgetötet werden kann. Darüber hinaus können differenzierte CTLs Zytokine hauptsächlich Interferon-γ (ein Typ II Interferon) ausschütten, das Phagozyten (Fresszellen) aktiviert, die den Zellschrott, der im Rahmen der Entzündungsreaktion entstanden ist, abräumen. CTLs ähneln daher in ihrer Funktion den NK-Zellen – sind aber noch spezifischer, oder wenn sie so wollen, noch „tödlicher“.
Wir können daher hier schon einmal festhalten, dass für die Bekämpfung einer Virusinfektion vor allem die normale Funktion der NK-Zellen und der CD8 positiven T-Lymphozyten, aus denen sich im Rahmen der Immunantwort sog. zytotoxische T-Lymphozyten entwickeln, wichtig ist. Da
- weder Interferon-Präparate (Betaferon, Rebif, Avonex, Plegidy, Extavia), noch Glatitrameracetat (Copaxone, Clift),
- noch Dimethylfumarat (Tecfidera) oder Natalizumab (Tysabri)
die Funktion dieser beiden Zelltypen vermindern, ist es sehr unwahrscheinlich, dass die Anwendung dieser Medikamente zur Therapie der MS, die Fähigkeit von MS-Patienten zur Virusabwehr beeinflussen. Bei den übrigen Medikamenten, die direkt in die zelluläre Immunität eingreifen, muss die Betrachtung etwas differenzierter vorgenommen werden, was ich in den Folgeartikeln versuchen werde.
Zu guter Letzt möchte ich den Beitrag noch mit der Erklärung abschließen, wie dann nach erfolgreicher Virusabwehr eine (lang) anhaltende Immunität entsteht. Diese beruht auf der Bildung von Antikörpern gegen Bestandteile des Virus. Diese Antikörper (bzw. die Zellen, die Antikörper produzieren) werden in den Keimzentren der Lymphknoten durch die Interaktion von CD4 positiven T-Helfer Zellen und B-Lymphozyten gebildet. Die Antikörper erreichen allerdings Viren nur extrazellulär – wenn die Viren bereits in die Zellen eingedrungen sind und begonnen haben, sich in der Zelle zu vermehren, sind sie für Antikörper nicht zugänglich. Demnach ist die Schutzwirkung der Antikörper insbesondere nach einer vorherigen Infektion (oder Impfung ) gegeben. Antivirale Antikörper binden in diesem Fall sofort an die Virushüll- oder Kapsidproteine und wirken dann als neutralisierende Antikörper, die die Anheftung von Viren an die Zellmembran und damit auch den Eintritt in Wirtszellen verhindern. Damit verhindern Antikörper sowohl die Infektion als auch die Ausbreitung von Zelle zu Zelle.
Wenn aber noch keine Immunität besteht (wie jetzt bei der Corona-Epidemie) sind Antikörper alleine bei einer bereits etablierten Infektion nicht in der Lage, das Virus von sich aus zu beseitigen. Das ist übrigens auch ein ganz wesentlicher Grund, warum ich in der derzeitigen Situation in Bezug auf B-Zell depletierende MS-Therapien wie Ocrelizumab (und Rituximab) relativ gelassen bin. Dieses Thema werde ich aber noch etwas ausführlicher in einem der nächsten Beiträge erläutern.









Vielen Dank für ihren Beitrag.
Eine Frage bleibt für mich jedoch offen.
Ist es nicht so, dass in einigen Fällen das Immunsystem, sobald es mit (neuartigen) Viren zu tun bekommt, absoluten Alarm schlägt, und dadurch die Schubwahrscheinlichkeit erhöht wird.
Und insofern eine Ansteckung doch wieder gravierende Folgen haben könnte.
Es wäre schön, wenn das Thema auch einmal beleuchtet wird.
Vielen Dank.
Sehr geehrter Herr Professor Mäurer,
vielen Dank, dass Sie sich die Mühe machen, uns MS-Patienten in die Funktionsweise des Immunsystems/der Immunsysteme einzuführen. In dieser coronadominierten Zeit freue ich mich über jede noch so kleine fundierte Information, die der Verunsicherung entgegenwirkt.
Zähle ich zu den Risikopatienten aufgrund von Immunsuppression? Das ist die Frage, die viele MSler umtreibt. Für ein paar Medikamente haben Sie ja schon vorsichtig Entwarnung gegeben („sehr unwahrscheinlich“). Ich würde mich über Aussagen zu weiteren Präparaten, beispielsweise Lemtrada, sehr freuen.
Herzliche Grüße
Sali
Ich schließe mich Sali gerne an und bedanke mich für ihre Mühe und bitte sie auch um eine Einschätzung in Bezug auf Mavenclad (cladribin).
Vielen Dank und beste Grüße, Magdalena